Decapeptyl Semestral en el Tratamiento del Cáncer de Próstata Metastásico: Un Enfoque Integral
El cáncer de próstata hormonosensible metastásico (CPHSM) ha sido objeto de una profunda evolución en su abordaje terapéutico durante la última década. La estrategia clínica ha transitado de depender exclusivamente de la terapia de privación de andrógenos (ADT) tradicional a incorporar de manera significativa los nuevos inhibidores de la vía del receptor de andrógenos (ARPIs). Estos fármacos, que incluyen el acetato de abiraterona, enzalutamida, apalutamida y darolutamida, han demostrado una mejora sustancial en la supervivencia global de los pacientes con CPHSM, tanto cuando se administran en combinación con ADT como cuando se suman a la ADT y docetaxel.
La Era de los Inhibidores de la Vía del Receptor de Andrógenos (ARPIs)
Los estudios pivotales que condujeron a la aprobación de los ARPIs en el contexto del CPHSM emplearon pruebas de imagen convencionales para la identificación de las metástasis. Los resultados de estos ensayos han revelado que los pacientes que responden de manera óptima al tratamiento, caracterizados por una rápida y pronunciada disminución de los niveles de PSA (antígeno prostático específico), se convierten en supervivientes a largo plazo. Se estima que estos individuos pueden alcanzar una supervivencia global del 70% al 80% a los 5 años. Esta prolongada expectativa de vida implica que dichos pacientes estarán expuestos a estos fármacos durante períodos considerablemente extensos, lo que subraya la importancia de comprender a fondo su mecanismo de acción, eficacia y perfil de seguridad.
Comprendiendo los Andrógenos y su Rol en el Cáncer de Próstata
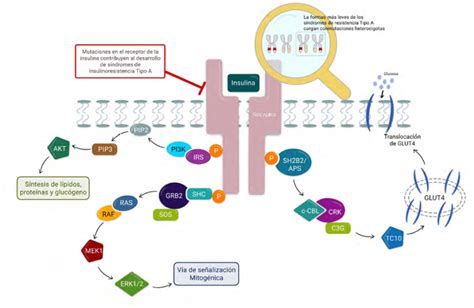
Para abordar el tratamiento del cáncer de próstata, es fundamental comprender el papel de las hormonas, en particular los andrógenos. Las hormonas son mensajeros químicos producidos por las glándulas del cuerpo que regulan diversas funciones celulares y orgánicas. Los andrógenos, comúnmente conocidos como hormonas sexuales masculinas, son cruciales para el desarrollo y mantenimiento de las características masculinas, siendo la testosterona y la dihidrotestosterona (DHT) los más abundantes en los hombres. Estas hormonas son esenciales para el crecimiento y funcionamiento normal de la próstata, una glándula del sistema reproductor masculino que contribuye a la producción de semen.
Sin embargo, los andrógenos también actúan como "combustible" para el crecimiento de los cánceres de próstata. Se unen al receptor de andrógeno (AR), una proteína ubicada en las células prostáticas. Al activarse, el AR estimula la multiplicación celular, tanto en el tejido prostático normal como en las células cancerosas. Una vez activado, el complejo AR promueve la expresión de genes específicos que impulsan la proliferación celular prostática. La testosterona se produce predominantemente en los testículos, con una contribución menor de las glándulas suprarrenales.
La Terapia Hormonal: Un Pilar en el Tratamiento del Cáncer de Próstata
Los cánceres de próstata, en sus etapas iniciales, dependen de los andrógenos para crecer. Las terapias hormonales buscan contrarrestar esta dependencia disminuyendo las concentraciones de andrógenos o bloqueando su acción, lo que puede frenar el crecimiento tumoral. Esta dependencia de los andrógenos es la razón por la cual estos tumores se clasifican como cáncer de próstata sensible a la castración (CPH) o sensible a las hormonas. Históricamente, estos cánceres también se han descrito como dependientes de andrógenos, sensibles a andrógenos o refractarios a hormonas.
Con el tiempo, la mayoría de los cánceres de próstata desarrollan resistencia a la terapia hormonal, evolucionando a un estado de cáncer de próstata resistente a la castración (CPRC). En esta fase, los tumores continúan creciendo a pesar de los bajos niveles de andrógenos en el cuerpo. Aunque anteriormente se utilizaban términos como "resistentes a las hormonas" o "independientes de andrógenos", la comprensión actual sugiere que el crecimiento de estos tumores no es completamente independiente de los andrógenos, sino que han desarrollado mecanismos para seguir utilizándolos, incluso en concentraciones muy bajas.
Estrategias de Terapia de Privación de Andrógenos (TPA)
La terapia hormonal para el cáncer de próstata se centra en inhibir la producción o el uso de andrógenos. La Terapia de Privación de Andrógenos (TPA) es el enfoque terapéutico más común y el primero que reciben la mayoría de los hombres con cáncer de próstata. La TPA se puede administrar de diversas maneras:
Orquiectomía (Castración Quirúrgica): Es una cirugía para extirpar uno o ambos testículos. Al eliminar la principal fuente de testosterona, se logra una reducción del 90% al 95% en los niveles sanguíneos de esta hormona. Si bien es una solución permanente y coste-efectiva, muchos hombres encuentran difícil aceptar la extirpación de los testículos y las implicaciones estéticas y psicológicas asociadas.
Agonistas de la Hormona Liberadora de Hormona Luteinizante (LHRH) / Agonistas de GnRH: Estos medicamentos son proteínas sintéticas que imitan la acción de la LHRH natural. Actúan sobre la hipófisis, impidiendo la secreción de hormona luteinizante (LH). La LH es la señal que estimula a los testículos a producir andrógenos. Inicialmente, los agonistas de LHRH pueden provocar un aumento temporal de la LH y, por ende, de la testosterona (conocido como "repunte de testosterona"), lo que puede empeorar temporalmente los síntomas. Sin embargo, la exposición continua a estos agonistas suprime la producción de LH, llevando a una reducción drástica de los niveles de testosterona. Ejemplos aprobados en EE. UU. incluyen leuprorelida, goserelina y triptorelina. Este método se conoce como castración médica o química y es reversible al suspender el tratamiento.
Antagonistas de la Hormona Liberadora de Hormona Luteinizante (LHRH) / Antagonistas de GnRH: A diferencia de los agonistas, los antagonistas de LHRH se unen directamente a los receptores de LHRH en la hipófisis, bloqueando la acción de la LHRH sin causar un aumento inicial de la testosterona. Esto permite una reducción más rápida de los niveles de testosterona y evita el "repunte de testosterona". El acetato de degarelix y el relugolix son antagonistas de LHRH aprobados para el tratamiento del cáncer de próstata avanzado.
Manejo Médico de la Miomatosis Uterina Antagonistas de GnRH
Tratamientos que Inhiben la Actividad de los Andrógenos
Cuando la TPA por sí sola deja de ser efectiva, se recurre a tratamientos que actúan directamente sobre los andrógenos o sus receptores:
Inhibidores del Receptor de Andrógeno (ARPIs): Estos medicamentos compiten con los andrógenos por su unión al receptor de andrógeno (AR). Al bloquear esta unión, impiden que los andrógenos estimulen el crecimiento de las células cancerosas. Comúnmente, se utilizan en combinación con la TPA (bloqueo combinado de andrógenos, bloqueo completo de andrógenos, bloqueo máximo de andrógenos o bloqueo total de andrógenos) para lograr una supresión más profunda de la señalización androgénica. Los ARPIs se dividen en dos generaciones:
- Primera Generación: Flutamida, bicalutamida y nilutamida.
- Segunda Generación: Enzalutamida, apalutamida y darolutamida. Estos fármacos se unen al AR con mayor afinidad y especificidad, ofreciendo una mayor eficacia. La darolutamida destaca por su limitada penetración en la barrera hematoencefálica, lo que se traduce en menos efectos secundarios a nivel del sistema nervioso central. Los ARPIs de segunda generación se administran por vía oral.
Inhibidores de la Síntesis de Andrógenos: Estos medicamentos interfieren con la producción de andrógenos en diversos tejidos del cuerpo, no solo en los testículos. La enzima clave en esta vía es la CYP17, esencial para la producción de testosterona en testículos, glándulas suprarrenales y células prostáticas. Al inhibir la CYP17, estos fármacos logran una reducción de los niveles de testosterona aún mayor que la TPA convencional.
- Abiraterona: Se administra por vía oral, a menudo en combinación con prednisona, para el cáncer de próstata metastásico, tanto sensible a la castración como resistente a la castración. La abiraterona no detiene la producción de testosterona en los testículos, por lo que en hombres que no han sido sometidos a orquiectomía, es necesario continuar con un agonista o antagonista de LHRH.
- Ketoconazol: Originalmente un antifúngico, también inhibe la producción de andrógenos en las glándulas suprarrenales. Se utiliza con menos frecuencia que la abiraterona.
Aplicaciones de la Terapia Hormonal en Diferentes Estadios del Cáncer de Próstata
La terapia hormonal se emplea en diversas situaciones clínicas del cáncer de próstata:
- Cáncer de Próstata en Estadio Temprano con Riesgo Intermedio o Alto de Recidiva: En hombres que reciben radioterapia para la enfermedad localizada, la TPA se añade frecuentemente para reducir el riesgo de que el cáncer reaparezca.
- Cáncer de Próstata en Recaída o Recidivante: La terapia hormonal es a menudo el tratamiento principal para pacientes cuya enfermedad ha regresado después de un tratamiento previo (cirugía o radiación). Se recomienda especialmente en casos de recurrencia sintomática (evidenciada por pruebas de imagen como PET-PSMA) y puede considerarse en "recidivas bioquímicas" (aumento del PSA sin síntomas evidentes), sobre todo si el aumento es rápido.
- Cáncer de Próstata Avanzado o Metastásico Sensible a la Castración (CPHSM): Históricamente, la TPA sola era el estándar. Actualmente, se administra en combinación con ARPIs (abiraterona, enzalutamida, apalutamida) o con docetaxel y un ARPI de segunda generación como abiraterona o darolutamida. En casos de metástasis extensas, se puede emplear una combinación de TPA, quimioterapia y otro agente hormonal.
Desescalada Terapéutica y Consideraciones en Pacientes de Edad Avanzada
En el escenario actual del tratamiento del CPHSM, la desescalada terapéutica (reducción de la intensidad o duración del tratamiento) es un tema de creciente interés. Si bien los estudios pre-ARPIs sugirieron que la TDA convencional intermitente no era inferior a la continua en términos de supervivencia global, con posibles beneficios en mortalidad cardiovascular y un pequeño impacto negativo en mortalidad específica por cáncer, no existe evidencia concluyente que respalde la intermitencia en el contexto actual con ARPIs. Por lo tanto, la desescalada solo debe considerarse en casos donde el tratamiento sistémico continuo represente un riesgo inasumible (eventos cardiovasculares agudos o alto riesgo) o genere toxicidad intolerable.
La decisión de retirar un ARPI, incluso en pacientes con buena respuesta, debe ser cuidadosamente sopesada. Solo aquellos pacientes sin factores de mal pronóstico, preferiblemente con CPHSM de bajo volumen, que estén motivados y plenamente informados de los riesgos potenciales de la interrupción, deberían ser considerados para la desescalada.
En pacientes de edad avanzada, el impacto de los ARPIs en la supervivencia global puede ser menor. Aunque estos fármacos pueden disminuir la mortalidad específica por cáncer, el posible aumento de la mortalidad cardiovascular en esta población puede neutralizar o atenuar el beneficio en la supervivencia global.
El Rol de Decapeptyl Semestral en el Tratamiento
El Decapeptyl, cuyo principio activo es la triptorelina, es un análogo sintético de la GnRH. Su mecanismo de acción, como agonista de la GnRH, implica la estimulación inicial de la secreción de FSH y LH, seguida de una disminución en tratamientos a largo plazo. Esta supresión inhibe la producción de estrógenos y andrógenos en ovarios y testículos, respectivamente.
En hombres con cáncer de próstata hormonosensible, la triptorelina induce una castración química, reduciendo los niveles de testosterona. El Decapeptyl está disponible en diferentes formatos: diario (0.1mg/1ml), mensual (3.75mg), trimestral (11.25mg) y semestral (22.5mg). La elección del formato depende de la estrategia médica. El formato semestral, con una dosis de 22.5mg, ofrece una administración menos frecuente, lo que puede mejorar la adherencia y conveniencia para el paciente en tratamientos de larga duración.
Si bien el Decapeptyl es un componente valioso en el manejo del cáncer de próstata, su uso, al igual que otras terapias de privación de andrógenos, conlleva efectos secundarios. Estos pueden incluir:
- Hipoestrogenismo (en mujeres) / Hipogonadismo (en hombres): Disminución de los niveles hormonales, que puede manifestarse como sofocos, pérdida de libido, disfunción eréctil, fatiga, pérdida de masa muscular, aumento de peso, cambios de humor y depresión.
- Salud Ósea: El hipogonadismo prolongado puede conducir a una disminución de la densidad ósea, aumentando el riesgo de fracturas.
- Efectos Locales: Irritación en el sitio de la inyección, que se puede mitigar rotando el punto de punción.
- Otros: Dolor abdominal, náuseas, cefalea, y en raras ocasiones, problemas de memoria o concentración.
Es crucial una monitorización rigurosa y una comunicación abierta entre el paciente y el equipo médico para gestionar estos efectos secundarios y optimizar la calidad de vida durante el tratamiento.
Nuevas Fronteras Terapéuticas: Radiofármacos y Más Allá
El tratamiento del cáncer de próstata resistente a la castración ha experimentado avances significativos con la introducción de nuevas modalidades terapéuticas:
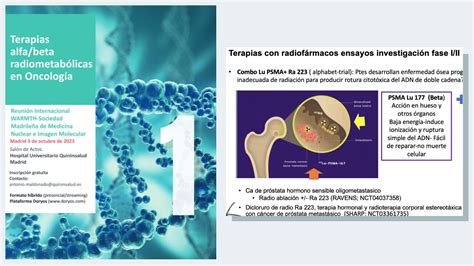
- Radiofármacos:
- Dicloruro de Radio Ra 223 (Xofigo): Este agente emisor de partículas alfa se acumula selectivamente en las metástasis óseas, que son comunes en el CPRC. Al emitir radiación alfa, ejerce un efecto citotóxico localizado, destruyendo las células cancerosas en el hueso. Ha demostrado mejorar la supervivencia global, retrasar la aparición de eventos óseos sintomáticos y mejorar la calidad de vida en pacientes con metástasis óseas sintomáticas y sin metástasis viscerales.
- Lutecio Lu 177 Vipivotida Tetraxetán (Pluvicto): Este radiofármaco se dirige a las células de cáncer de próstata, se une a ellas y emite radiación para destruirlas.
- Inhibidores de PARP: Medicamentos como rucaparib, olaparib, talazoparib y niraparib (en combinación con abiraterona) están aprobados para tratar CPRC metastásico con mutaciones genéticas específicas que afectan la reparación del ADN en las células cancerosas.
- Inmunoterapia: La vacuna de células Sipuleucel-T (Provenge) es un ejemplo de inmunoterapia utilizada en el tratamiento del CPRC.
El Futuro: Personalización y Optimización del Tratamiento
La investigación continúa explorando estrategias para optimizar la terapia hormonal, incluyendo la determinación de la duración óptima del tratamiento y el momento más adecuado para iniciar o suspender la terapia. La terapia intermitente, donde el tratamiento se administra en ciclos con periodos de descanso, se ha investigado con el objetivo de demorar la resistencia a la terapia hormonal y mejorar la calidad de vida. Sin embargo, aún se requiere más evidencia para establecer su beneficio comparado con la terapia continua.
La comprensión de las vías moleculares del cáncer de próstata y la identificación de biomarcadores predictivos son cruciales para la personalización del tratamiento. El objetivo es asegurar que cada paciente reciba la terapia más efectiva y con el menor perfil de toxicidad posible, mejorando así la supervivencia y la calidad de vida en esta compleja enfermedad. La investigación sobre compuestos que puedan disociar los grupos de células tumorales circulantes (CTC) y suprimir el desarrollo de metástasis abre nuevas vías para abordar la enfermedad metastásica de manera innovadora.
La colaboración internacional y la participación en ensayos clínicos son fundamentales para seguir avanzando en el conocimiento y manejo del cáncer de próstata metastásico, ofreciendo esperanza y mejores resultados a los pacientes afectados.
tags: #decapeptyl #semestral #frena #una #metastasis